ニュース 医薬 作成日:2014年5月6日_記事番号:T00050144
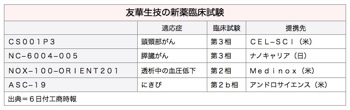
友華生技医薬(オリエント・ユーロファーマ)が開発した▽頭頸部がん▽膵臓(すいぞう)がん▽透析時低血圧▽にきび──を対象とする新薬4項目は現在、米食品医薬品局(FDA)の承認に向けた第2〜3相臨床試験に入っている。6日付工商時報が報じた。
友華生技の蔡正弘董事長は「新薬の開発リスクを抑えるため、常に海外メーカーとの提携による研究開発(R&D)態勢を採っており、当社はアジアにおける臨床試験と販売を担当している」と説明。4項目の新薬については2017〜20年に業績貢献が始まるとの見通しを示した。
なお4項目の新薬のうち、進度が最も早い頭頸部がん治療薬については米CEL-SCI社と提携して世界での第3相臨床試験を進めている。
また日本の創薬ベンチャー、ナノキャリア(本社・千葉県柏市、中冨一郎社長)を共同開発パートナーとする膵臓がん治療薬「NC-6004」については、今年第3相臨床試験に入り、17年に完了する予定だ。
統一企業(ユニプレジデント)傘下の統一生命科技と合弁で立ち上げた米アンドロサイエンスが開発したにきび治療薬「ASC-19」も既に第2b相臨床試験を終えている。

台湾のコンサルティングファーム初のISO27001(情報セキュリティ管理の国際資格)を取得しております。情報を扱うサービスだからこそ、お客様の大切な情報を高い情報管理手法に則りお預かりいたします。

ワイズコンサルティンググループ
威志企管顧問股份有限公司
Y's consulting.co.,ltd
中華民国台北市中正区襄陽路9号8F
TEL:+886-2-2381-9711
FAX:+886-2-2381-9722